美國生技業在景氣與資本市場壓力下,轉向以高價罕病與中樞神經藥物博取成長。Axsome Therapeutics(AXSM)押寶抗憂鬱藥AUVELITY擴張至阿茲海默症激動症,Capricor Therapeutics(CAPR)則在與合作夥伴翻臉之際,孤注一擲推進Duchenne肌營養不良新療法deramiocel,兩家公司同樣站上監管、商業與法律風險交會口。
美股生技板塊今年再度聚焦高單價、高風險的新藥賭局,其中以中樞神經系統與罕病治療最受關注。從Axsome Therapeutics(AXSM)到Capricor Therapeutics(CAPR),兩家公司分別把賭注押在阿茲海默症激動症與Duchenne肌營養不良(DMD),共同特色是臨床數據亮眼、商業空間巨大,但同時也必須穿越FDA審查、支付方壓力與合作關係撕裂的多重考驗。
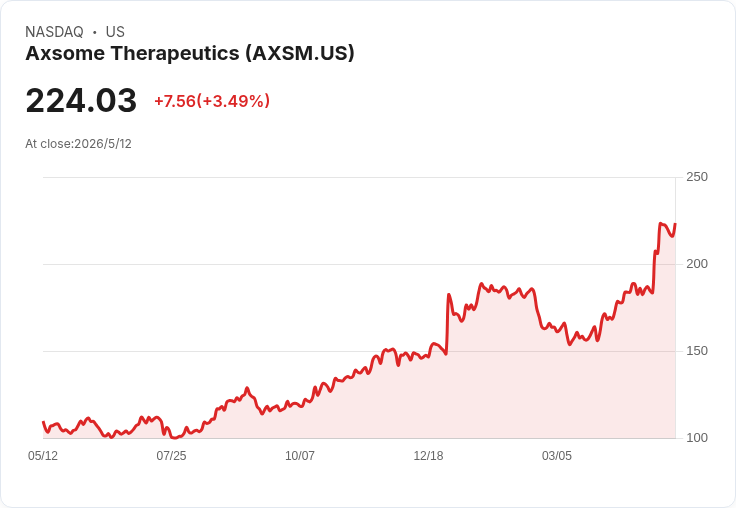
首先登場的是專攻CNS疾病的Axsome Therapeutics。公司高層公開表示,已為6月在阿茲海默症激動症領域推出AUVELITY做最後準備,試圖在原本已獲准的重鬱症(MDD)適應症基礎上,開啟第二成長引擎。營運團隊強調,AUVELITY在MDD市場已累積14季銷售經驗,目前在整體抗鬱藥市場占比約0.2%,但年化銷售額已超過6億美元,並擁有86%健保給付涵蓋率,其中56%屬於第一線或第一替換用藥資格,顯示處方滲透仍在起步階段就展現放大效應。
為了抓住阿茲海默症激動症的新需求,Axsome選擇大幅加碼一線銷售火力。公司原先以約160名業務推進MDD市場,歷經兩度擴編至300人,如今為迎接新適應症,已將業務團隊拉高至630人。營運長Mark Jacobson指出,看好長照機構成為兩個適應症的交集戰場,因為「50%到80%的長照住民有憂鬱症」,而阿茲海默症激動症患者亦高度集中在這個通路;未來每一位業務代表都將同時肩負MDD與阿茲海默症激動症的開發任務,依不同醫師類型與院所屬性精準分配。
從產品本身競爭力來看,Axsome刻意凸顯AUVELITY在阿茲海默症激動症的差異化優勢。Jacobson表示,藥物機轉同時鎖定NMDA與sigma-1受體,與現行此族群常用的標準與非標準用藥顯著不同,臨床證據除顯示在2到3週就能看到症狀改善,亦具備預防復發的長期數據。更關鍵的是,針對這個新族群的標籤沒有「黑框警語」,也未見鎮靜、死亡率或跌倒風險訊號,最常見副作用僅眩暈與消化不良,試圖在安全與耐受性上形成區隔。
在支付面,財務長Nick Pizzie預估約八成阿茲海默症激動症處方會落在Medicare Part D,並指出公司目前在Part D達到100%覆蓋,當中75%的投保人無需事前授權就能以第一線或第一替換用藥身分開立,其餘多數只需確認適應症即可。由於Part D禁止共付額補助,公司反而預期淨價將優於一般商業保險,有利於維持獲利空間。配合自去年第四季起啟動的電視與數位直效行銷(DTC),Axsome正一面擴充MDD在初級照護診間的滲透,一面鋪陳阿茲海默症適應症上市後的拉貨力道。
相較之下,Capricor Therapeutics走的是完全不同、卻同樣高張力的道路。公司主力候選藥deramiocel(又稱CAP-1002)鎖定罕病DMD,且已將生死關鍵押在今年8月22日的FDA PDUFA法定審查期限。執行長Linda Marbán形容,公司正處在「真正關鍵的時刻」,不僅要回應FDA對去年7月完整回覆信(CRL)的意見,也同時為商業化布建產線與銷售體系。
在科學證據上,Capricor祭出HOPE-3三期試驗作為反攻本錢。該試驗納入106名患者,為多中心、隨機、雙盲、安慰劑對照設計,主要終點採用上肢功能量表PUL 2.0。Marbán表示,12個月時deramiocel在主要終點達成約54%疾病惡化減緩,p值0.029,所有預先控管第一型錯誤的次要終點也全部達統計顯著。針對本次BLA鎖定的心肌病適應症,左心室射出分率(LVEF)則顯示整體可評估族群約91%的疾病進展減緩,而在已確診心肌病子族群中,效果更擴大到約120%緩解、p值0.01。再加上心臟MRI顯示纖維化進展穩定、居家照護者拍攝的上肢影片客觀改善,以及超過800次靜脈注射、最長連續治療五年的安全數據,公司試圖向FDA傳遞「高效且耐受良好」的明確訊號。
不過,Capricor面臨的挑戰並不只來自監管。更戲劇性的衝突出現在商業合作戰線上。公司在5月7日對日本Nippon Shinyaku及其美國子公司NS Pharma提起訴訟,要求以加速程序撤銷先前簽訂的美國市場商業化與通路協議,並尋求初步禁制令,盼在FDA批准後得以自行或另尋夥伴配銷deramiocel。Marbán直言,爭議核心在於價格結構存在「根本性缺陷」,使得在Medicare、Medicaid與商業保險制度下,醫院與診所對每一劑恐面臨嚴重給付短缺,等同從制度上堵住病人取得療法之路,而非單純毛利高低的問題。
在長達一年多的協商無果後,Capricor選擇鋌而走險,準備收回完整商業主導權,即便代價可能是退還已收的5,000萬美元里程金。為了在最壞情境下仍能獨立上市,公司已在聖地牙哥建成自有GMP工廠並通過FDA預先查廠,初期產能可支應每年約200到250名患者、約1,000劑藥品,未來擴產到第二層樓後,目標放大到每年2,000到2,500名患者、約1萬劑供應。考量deramiocel屬超低溫鏈產品且須在冷凍前完成標籤,公司也正與FDA協商臨時標籤方案,以便提前量產。
從財務結構來看,Capricor手握約2.79億美元現金與有價證券,預估足以支撐營運至2027年第四季,即便目前尚未有產品收入、今年第一季仍錄得約3,390萬美元或每股0.59美元淨損。管理層坦言,近期費用大幅上升,主要用於支持BLA審查、擴充製造能力與組建商業團隊,同時也把部分資源轉向以外泌體(exosome)為基礎的後續產品線,雖然疫苗開發暫時淡出,但仍保留治療性應用與國際拓展計畫。
綜觀Axsome與Capricor兩家公司的策略,可以看到美國生技產業在資本市場偏好疊加醫療需求轉變之下,正快速朝「少量高價、高證據門檻」的新商業模式集結。前者倚賴標籤擴張與大規模商業部署,在廣泛的CNS市場尋求疊加效應;後者則用罕病高未滿足需求與臨床優勢,試圖在小族群中創造高單價藥品價值。然而,無論是哪一條路,最終仍繫於FDA的風向、保險給付與醫師採用速度,更要承受合作關係破裂與法律戰的額外變數。對投資人而言,這是一場可能開啟數十億美元長期現金流、也可能因一紙決定而腰斬估值的「高風險高報酬」押注,如何評估科學數據與商業執行力,將成為決定是否進場的關鍵。
點擊下方連結,開啟「美股K線APP」,獲得更多美股即時資訊喔!
https://www.cmoney.tw/r/56/9hlg37
本網站所提供資訊僅供參考,並無任何推介買賣之意,投資人應自行承擔交易風險。

 發表
發表


 我的網誌
我的網誌